Alfa-pinen
I dagens verden er Alfa-pinen blevet et emne af stor relevans og interesse. Siden starten har Alfa-pinen vakt nysgerrighed og undersøgelse hos både forskere, eksperter og hobbyfolk. Dens indflydelse strækker sig gennem historien, og dens indvirkning kommer til udtryk på forskellige områder af samfundet. I denne artikel vil vi udforske betydningen og vigtigheden af Alfa-pinen fra forskellige perspektiver, såvel som dets udvikling over tid. Vi vil lære om dens indflydelse på kultur, teknologi, politik, økonomi og andre aspekter af hverdagen, og vi vil analysere, hvordan Alfa-pinen fortsætter med at udøve sin indflydelse i dagens verden.
| Alfa-pinen | ||||
|---|---|---|---|---|
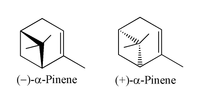
| ||||
| Generelt | ||||
| Systematisk navn | (1S,5S-2,6,6-trimethyl bicyclohept-2-ene ((-)-Pinene) | |||
| Andre navne | α-pinen | |||
| Molekylformel | C10H16 | |||
| Molmasse | 136.23 | |||
| CAS nummer | (uspecificeret) (+)-α-Pinen (-)-α-Pinen)] | |||
| SMILES | CC1(C)C2CC1C(C)=CC2 | |||
| Egenskaber | ||||
| Massefylde | 0.858 g/mL | |||
| Opløselighed i ætanol | blandbart | |||
| Smeltepunkt | -64 °C | |||
| Kogepunkt | 155 °C | |||
| Specifik rotation D | -50.7° | |||
| Sikkerhed | ||||
| NFPA 704 |
| |||
| R-sætninger | R10, R20/21/22, R36/37/38, R43, R51 | |||
| S-sætninger | S16, S26, S36, S37, S60, S61 | |||
| RTECS nummer | DT7000000 (uspec. isomer) | |||
| Hvis ikke andet er angivet, er data givet for stoffer i standardtilstanden (ved 25 °C, 100 kPa) | ||||
α-Pinen er en organisk forbindelse som hører til terpenerne, det er den ene af to isomerer af pinen. Det er en alken som indeholder en fireleddet ring. Den findes i olier fra mange arter af nåletræer, specielt fyr (deraf navnet: fyr på engelsk: pine). Begge enantiomerer kendes fra naturen; 1S,5S- eller (-)-α-pinen er mest almindelig i europæiske fyrretræer, mens 1R,5R- eller (+)-α-isomeren er mest almindelig i Nordamerika. Den racemiske blanding findes i nogle olier, f.eks. eukalyptusolie. α-Pinen findes også i sassafrasolie.
Kemiske egenskaber
Reaktivitet
Den fireleddede ring i α-pinen 1 gør denne forbindelse til en reaktiv kulstofforbindelse som er tilbøjelig til at rearrangere sit kulstofskelet. Forsøg på at hydrere α-pinen eller addere hydrogenhalider til dobbeltbindingen resulterer i stedet i rearrangerede produkter, specielt under sure omstændigheder. Men koncentreret svovlsyre og ætanol er hovedprodukterne terpineol 2 og dennes ætylæter 3, mens iskold eddikesyre resulterer i den tilsvarende acetatester 4. Med fortyndede syrer er terpinhydrat 5 hovedproduktet.

Med en molækvivalent vandfri saltsyre og i tilstedeværelse af Diethylether dannes additionsproduktet 6a ved lav temperatur. Denne forbindelse er dog meget ustabil. Ved stuetemperatur, eller uden æter, er hovedproduktet bornylklorid 6b, sammen med små mængder af fenkylalkohol 6c. I mange år blev 6b kaldt pinenhydroklorid, indtil det blev bekræftet at den er identisk med bornylklorid fra kamfen (den kaldes også kunstig kamfer). Ved overskud af HCl dannes den akirale forbindelse 7 (dipentenehydroklorid) som hovedprodukt sammen med 6b. Oximforbindelsen 8 dannes i nitrosylkloride og efterfølgende base, denne oxim kan reduceres til "pinylamin" 9. Både 8 og 9 er stabile forbindelser som indeholder fireleddede ringe, og de benyttes til at identificere pinenskelettet.
Nogle reagenser som f.eks. iod eller fosfortriklorid får α-pinen til at danne den aromatiske forbindelse p-cymen 10.
Brug
α-pinen bruges i nogle farvestoffer, og er blevet identificeret som flygtige stoffer i nogle tryksager som f.eks. reklamer og kataloger. α-pinen kan polymeriseres til α-pinenpolymer, der er et insekticid.
Sikkerhed
α-pinen er allergifremkaldende og kan give allergisk kontakteksem.
Litteratur
- Simonsen, J. L. (1957) The Terpenes (2nd edition) Vol. 2 Cambridge:Cambridge University Press, pp 105-191.
- Richter, G. H. (1945) Textbook of Organic Chemistry, 2nd ed., John Wiley & Sons., New York, PP 663-666.
- Ruzicka & Trebler, Helv. Chim. Acta. 1921, 4, 566.